March 22, 2017 / 22. März 2017
| Introduction | Einleitung |
|---|---|
| First I would like to remark that chemistry is still a relatively young science. Its roots lie in Alchemy [1]. In the 17th and 18th century the knowledge base of Alchemists increased such that it became possible to make rational conclusions from the observations. But even today, centuries after the beginnings of chemical scientific research some experts in chemistry still refuse to call it a mature science. | Zunächst möchte ich vorausschicken, dass die Chemie immer noch eine junge Wissenschaft ist. Ihre Wurzeln liegen in der Alchemie [1]. Im 17. und 18. Jahrhundert nahm das Wissen der Alchemisten in grossem Masse zu, so dass sie damit beginnen konnten, rationale Schlüsse aus ihren Beobachtungen zu ziehen. Aber sogar heute, Jahrhunderte nach den Anfängen der wissenschaftlichen, chemischen Forschung gibt es Experten in der Chemie, die es immer noch ablehnen, die Chemie als eine reife Wissenschaft zu bezeichnen. |
| In organic chemistry, which is the chemistry focused on carbon based chemical compounds, there is a vast amount of known reactions [2]. The catalogue of reactions is large, such that practically any imaginable, more or less stable organic molecule could be produced synthetically. Organic chemistry has grown up quite a lot. In inorganic chemistry which takes care of the other elements (main group metals, transition metals, half metals, non metals) the situation is different. Many producible compounds are still unknown and their chemical properties rarely could be predicted. | In der organischen Chemie, der Chemie rund um Kohlenstoffbasierende chemische Verbindungen, sind eine grosse Menge an Reaktionen bekannt [2]. Die Liste an Reaktionen ist derart lang, dass praktisch jedes vorstellbare und einigermassen stabile, organische Molekül synthetisch hergestellt werden kann. Die organische Chemie ist diesbezüglich durchaus erwachsen geworden. In der anorganischen Chemie, die sich um die anderen Elemente kümmert (Hauptgruppen-Metalle, Übergangsmetalle, Halbmetalle, Nichtmetalle), ist die Situation eine andere. Dort sind noch sehr viele möglichen Verbindungen unbekannt, auch Stoffeigenschaften können nur selten passend vorhergesagt werden. |
| The first technically produced chemical | Die erste grosstechnisch hergestellte Chemikalie |
|---|---|
| The first technically produced substances were inorganic ones. The mineral acid sulphuric acid [3], which historically was called oil of vitriol, was the first chemical to be produced in larger quantities. Before the "Lead Chamber Process" [4] was discovered and established from 1746 on, sulphuric acid was produced via the more expensive "Vitriol Process" [5]. The first production site using the Lead Chamber Process was located in Birmingham, England [6], where the production began under the lead of John Roebuck [7]. In Switzerland, the first production plant of Sulfuric acid was constructed in Winterthur and operated from 1778 on [8]. | Die erste grosstechnisch hergestellten Substanzen waren anorganische. Die Mineralsäure Schwefelsäure [3], teilweise auch Monothionsäure oder Vitriolöl genannt, war die erste Chemikalie, die in grösseren Mengen hergestellt werden konnte. Bevor das Bleikammerverfahren [4] entdeckt und ab 1746 eingeführt wurde, wurde Schwefelsäure über das aufwendigere Vitriolverfahren [5] gewonnen. Die erste Produktionsanlage, die den Bleikammerprozess nutzte, wurde im englischen Birmingham [6] aufgebaut und unter der Leitung von John Roebuck betrieben [7]. In der Schweiz wurde die erste Produktionsanlage für Schwefelsäure in Winterthur errichtet und ab 1778 betrieben [8]. |
| The "Lead Chamber Process" is still used today in the cleaning of sulfurous smoke gases for example in refuse incinerator plants. | Das "Bleikammerverfahren" wird heute noch genutzt in der Reinigung schwefelhaltiger Rauchgase, zum Beispiel bei Kehrichtverbrennungsanlagen. |
The Lead Chamber Process / Das Bleikammer Verfahren
| Now it gets rather technical. I am still not sure where I really will go with this steemit channel, probably I will not focus that much on chemical reactions in the next articles. But especially when I will write about historic experiments or progress in plant engineering I would like to show how difficult it often was to make progress and overcome difficulties. From a 21st century point of view, many of these difficulties seem to be ridiculous, but humanity is still facing similar ones in unprospected fields. | Nun wird es eher technisch. Da ich noch nicht weiss, wo ich mit diesem Kanal genau hin möchte, tue ich das einmal. In folgenden Artikeln wird sich das eventuell nicht wiederholen. Allerdings möchte ich in Artikeln über historische Experimente oder Fortschritte im Aufbau chemischer Produktionsanlagen zeigen, wie schwierig es oft war, Fortschritte zu erzielen und die auftretenden Schwierigkeiten zu überwinden. Betrachtet man sich diese aus der Perspektive 21. Jahrhunderts, mögen viele damalige Schwierigkeiten lächerlich anmuten, allerdings sieht sich die Menschheit heute in anderen, noch nicht erkundeten Gebieten, mit ähnlichen Unwegbarkeiten konfrontiert. |
|---|
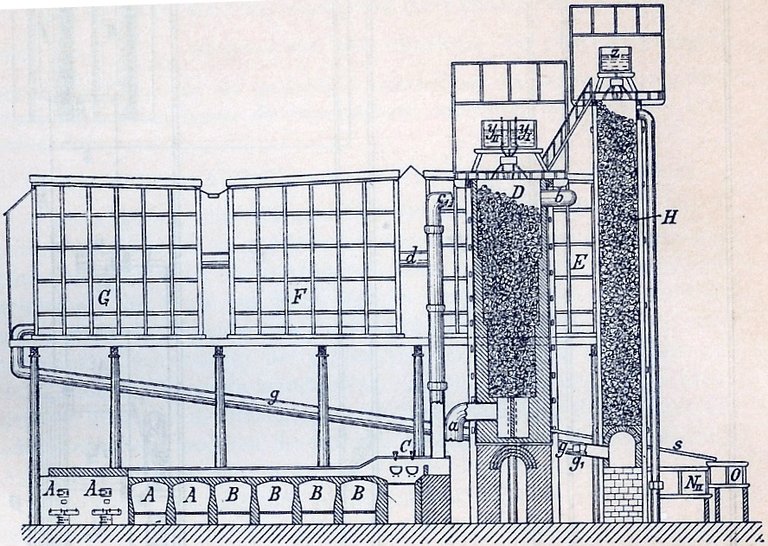
| Part | Description | Beschreibung [10] |
|---|---|---|
| A,B | Roast ovens for Pyrite, iron(II) disulfide. | Röstöfen für Pyrit (FeS2), Eisen(II) Disulfid. |
| C | Salpeter oven with two shells for sulfuric acid and salpeter in order to release nitrous gases. | Salpeterofen mit 2 Schalen für Schwefelsäure und Salpeter zur Freisetzung nitroser Gase. |
| D | Glover turret, invented in 1859 by British Chemist John Glover (1817-1902) [11], widely used from 1871 on. Countercurrent of roast and nitrous gases | Gloverturm, vom britischen Chemiker John Glover (1817-1902) [11] 1859 erfunden, ab 1871 weitere Verbreitung. Gegenstrom von Röst- und nitrosen Gasen. |
| E,F,G | Lead Chambers | Bleikammern |
| H | Gay-Lussac Turret to capture nitrous gases, first used in 1842. Invented by French Chemist Joseph Louis Gay-Lussac (1778-1850) [12]. | Gay-Lussac-Turm, um nitrose Gase aufzufangen, ab 1842 eingesetzt. Erfunden vom französischen Chemiker Joseph Louis Gay-Lussac (1778-1850) [12]. |

| Illustration of a Lead Chamber Process Plant [9]. | Darstellung des Aufbaus einer Anlage für das Bleikammerverfahren [9]. |
|---|
| Part | Description | Beschreibung [10] |
|---|---|---|
| I,K | Steam Boiler | Dampfkessel |
| L | Compressed Air Pump | Druckluftpumpe |
| M | Pressure Tank | Druckkessel |
| N | Tanks for Glover-Acid (ca. 80 % Sulfuric acid) | Behälter für Gloversäure (ca. 80 %-ige Schwefelsäure) |
| O | Cooling Tube | Röhrenkühler |
| N | The reaction procedure | Der Prozessablauf |
|---|---|---|
| 1 | Sulfur dioxide is generated by burning elemental sulfur or by roasting pyritic ore (FeS2) in a current of air. | Schwefeldioxid wird durch das Verbrennen elementaren Schwefels oder durch das Rösten von Pyrit (FeS2) in einem Luftstrom gewonnen. |
| 2 | Nitrogen oxides are produced by decomposition of niter in the presence of sulfuric acid or hydrolysis of nitrosylsulfuric acid. | Stickoxide werden durch die Zersetzung von Niter (KNO3) in Präsenz von Schwefelsäure oder durch die Hydrolyse von Nitrosylschwefelsäure (NOHSO4) hergestellt |
|---|
| 3 | In the reaction chambers, sulfur dioxide and nitrogen dioxide dissolve in the reaction liquor. Nitrogen dioxide is hydrated to produce nitrous acid which then oxidizes the sulfur dioxide to sulfuric acid and nitric oxide. The reactions are not well characterized but it is known that nitrosylsulfuric acid is an intermediate in at least one pathway. The major overall reactions are the following ones. | In den Reaktionskammern lösen sich Schwefeldioxid und Stickstoffdioxid in der Reaktionsflüssigkeit. Stickstoffdioxit wird hydratisiert, um Schweflige Säure zu ergeben. Diese oxidiert das Schwefeldioxid zu Schwefelsäure und Salpetersäure. Diese Reaktionen wurden nicht besonders gut beschrieben, aber es ist bekannt, dass die Nitrosylschwefelsäure in mindestens einem Reaktionsweg als Intermediat fungiert. Die wichtigsten Reaktionen sind die folgenden. |
|---|
| 4 | Nitric oxide escapes from the reaction liquor and is subsequently reoxidized by molecular oxygen to nitrogen dioxide. This is the overall rate determining step in the process. | Salpetersäure entweicht aus der Reaktionsflüssigkeit und wird unmittelbar mittels Sauerstoff wieder zu Stickstoffdioxid oxidiert. Dieser Prozess bestimmt die Geschwindigkeit des ganzen Prozesses. |
|---|---|---|
| 5 | Nitrogen oxides are absorbed and regenerated in the process, and thus serve as a catalyst for the overall reaction. | Stickoxide werden im Prozess aufgefangen und regeneriert, sie dienen also als Katalysatoren für die gesamte Reaktion. |
| 6 | In the last step sulfur dioxide has to be oxidized to sulfuric acid which could be done using water and oxygen. However this process could not be done such that pure sulfuric acid results from it. An aqueous solution of sulfuric acid is obtained instead. Further purification can be achieved by removal of water via heating. | Im letzten Schritt muss das Schwefeldioxid zu Schwefelsäure oxidiert werden, was mithilfe von Wasser und Sauerstoff gelingt. Allerdings konnte der Prozess nicht so durchgeführt werden, dass reine Schwefelsäure gewonnen werden kann. Man erhält stattdessen eine wässrige Lösung davon. Gereinigt werden kann die Lösung etwa durch Entfernung von Wasser mittels Erhitzen. |
|---|
A few words on the Vitriol Process / Einige Worte zum Vitriolverfahren
| As already mentioned above, the Vitriol Process was the predecessor of the Lead Chamber Process. | Wie bereits erwähnt, ist das Vitriolverfahren der Vorgänger des Bleikammerverfahrens. |
|---|
| N | Description | Beschreibung |
|---|---|---|
| 1 | Iron(II) sulfate heptahydrate is oxidized to iron(iii) sulfate. | Eisen(II)-sulfat Heptahydrat wird zu Eisen(III)-sulfat oxidiert. |
| 2 | Iron(iii) sulfate is decomposed to iron(iii) oxide. | Eisen(III)-sulfat wird zu Eisen(III)-oxid zersetzt. |
|---|
| 3 | The obtained sulfur trioxide or Oleum is processed with water in order to obtain sulfuric acid. | Das bei der Zersetzung entstandene Schwefeltrioxid oder Oleum wird mit Wasser zu Schwefelsäure umgesetzt. |
|---|
Production of Sulfuric Acid today / Produktion von Schwefelsäure heute
| Today sulfuric acid is mainly produced from elementary sulfur, which is obtained from the desulfurization of crude oil and natural gas. It has to be oxidized twice. First to sulfur dioxide, second to sulfur trioxide. Sulfur trioxide is catalytically produced via a highly efficient process, named the Double Contact Process. The catalyst is [(VO)2O(SO4)4]4− and the yield can be pushed to at least 99,8 % [3]. Afterwards sulfur trioxide is transformed to sulfuric acid in concentrated sulfuric acid via disulfuric acid. | Heute wird Schwefelsäure hauptsächlich aus elementarem Schwefel hergestellt, der aus der Entschwefelung von Rohöl und Erdgas in riesigen Mengen anfällt. Dieser muss zweifach oxidiert werden. Zunächst zu Schwefeldioxid, dann zu Schwefeltrioxid welches katalytisch im hoch effizienten Dopelkontaktverfahren erhalten wird. Der Katalysator ist [(VO)2O(SO4)4]4− und die Ausbeute kann bis mindestens 99,8 % betragen [3]. Danach wird Schwefeltrioxid in konzentrierter Schwefelsäure via Dischwefelsäure zu Schwefelsäure umgesetzt. |
|---|
[9] Das Bild ist gemeinfrei. Es erschien in H. Ost, Lehrbuch der Technischen Chemie, Verlag von Robert Oppenheim, Berlin, 1890, S. 53. und wurde von Georg Lunge gezeichnet. Gefunden unter:
[10] Enzyklopädie der Technischen Chemie. Band 9. 2. Auflage, 1932, Prof. Dr. Fritz Ullmann.
[1] https://en.wikipedia.org/wiki/Chemistry
https://de.wikipedia.org/wiki/Chemie
[2] https://en.wikipedia.org/wiki/List_of_organic_reactions
https://de.wikipedia.org/wiki/Liste_von_Namensreaktionen
[3] https://en.wikipedia.org/wiki/Sulfuric_Acid
https://de.wikipedia.org/wiki/Schwefels%C3%A4ure
[4] https://en.wikipedia.org/wiki/Lead_chamber_process
https://de.wikipedia.org/wiki/Bleikammerverfahren
[5] https://de.wikipedia.org/wiki/Vitriolverfahren
[6] https://de.wikipedia.org/wiki/Chemische_Industrie#Geschichte
[7] https://en.wikipedia.org/wiki/John_Roebuck
https://de.wikipedia.org/wiki/John_Roebuck
[8] https://de.wikipedia.org/wiki/Laboratorium_(chemische_Fabrik)
https://de.wikipedia.org/wiki/Bleikammerverfahren
https://archive.org/details/EnzyklopadieDerTechnischenChemieBand9
[11] https://de.wikipedia.org/wiki/John_Glover_(Chemiker)
[12] https://en.wikipedia.org/wiki/Joseph_Louis_Gay-Lussac
https://de.wikipedia.org/wiki/Joseph_Louis_Gay-Lussac
Hello @saamychemistry,
Congratulations! Your post has been chosen by the communities of SteemTrail as one of our top picks today.
Also, as a selection for being a top pick today, you have been awarded a TRAIL token for your participation on our innovative platform...STEEM.
Please visit SteemTrail to get instructions on how to claim your TRAIL token today.
If you wish to not receive comments from SteemTrail, please reply with "Stop" to opt out.
Happy TRAIL!
Thank you for choosing me!
Added to my #history-trail - good luck, awesome post! Check our trail https://discord.gg/ve7tmJP
Thank you, both for the comment and for adding me to the #history-trail.
my pleasure - gern geschehen!
Congratulations @saamychemistry! You have completed some achievement on Steemit and have been rewarded with new badge(s) :
Click on any badge to view your own Board of Honor on SteemitBoard.
For more information about SteemitBoard, click here
If you no longer want to receive notifications, reply to this comment with the word
STOP