Приблизно століття минуло з того часу, як Александр Флемінг випадково відкрив пеніцилін у 1928 році, і гриби стали справжньою золотою жилою для створення ліків. Вони забезпечили лікування широкого спектру захворювань, від інфекцій та високого рівня холестерину до відторгнення органів і навіть раку.
Однак процес, за допомогою якого гриби синтезують деякі зі своїх найпотужніших сполук, залишається малозрозумілим. Це особливо стосується циклопентахромону – ключового будівельного блоку грибкових продуктів, чиї похідні демонструють перспективи в боротьбі з раком та зменшенні запалення, серед інших лікувальних властивостей.
Хоча хімікам вдалося досягти певного прогресу у створенні похідних хромону в лабораторних умовах, характерну структуру цієї молекули виявилося складно точно й надійно відтворити. «Дуже легко отримати версію, у якій хімічні зв'язки знаходяться не на своїх місцях або структура перевернута», — каже Шеррі Гао, доцент кафедри хімічної та біомолекулярної інженерії (CBE) і біоінженерії (BE) в Університеті Пенсильванії.
У новій статті, опублікованій у журналі Американського хімічного товариства, співробітники лабораторії Гао описали, як вони розшифрували природні «інструкції», а саме гени Penicillium citrinum – цвілі, яка зазвичай зустрічається на цитрусових, і виявили раніше невідомий фермент, що каталізує створення сполук, які містять циклопентахромон.
«Природа мала мільярди років для розробки шляхів створення цих сполук», — зазначає Гао, старший автор статті. «Тепер ми можемо запозичити інструменти природи для подальшого розвитку й дослідження цих сполук, що потенційно може призвести до створення нових лікарських препаратів».
Молекулярна головоломка
Особливість циклопентахромону полягає в його унікальній структурі, яка включає тріо вуглецевих кілець: два з шістьма атомами вуглецю й одне з п’ятьма. Подібно до риштувань, що використовуються для будівництва будівлі, ця серія кілець забезпечує структурну основу для багатьох біоактивних молекул.
Однак один із відомих хімічних попередників циклопентахромону має додатковий атом вуглецю, утворюючи три кільця однакового розміру. Як саме природа змінює цей хімікат, щоб створити структуру з іншою кільцевою будовою, коли такі кільця зазвичай стабільні, раніше ніколи не описувалося.
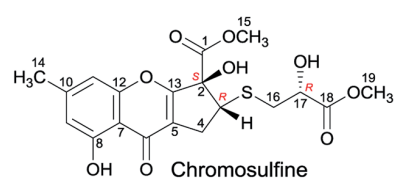
Один з таких представників Хромосульфін.
Хромосульфін — це природний продукт, який виділяється з грибів роду Penicillium. Він належить до класу хромонів і має унікальну хімічну структуру, що включає циклопентахромоновий скелет. Хромосульфін демонструє різноманітні біологічні активності, зокрема протипухлинну та протизапальну дію. Його хімічна структура складається з трьох конденсованих кілець: двох бензольних (шестичленних) та одного циклопентанового (п’ятичленного), а також містить сульфуровмісні функціональні групи. Дослідження хромосульфіну та його похідних тривають, оскільки вони можуть стати основою для розробки нових лікарських засобів.
Для з’ясування цього процесу було необхідно систематично вмикати й вимикати гени в P. citrinum, поки шлях не переривався, що дозволило б зрозуміти, які гени кодують функціонуючий фермент. «Це було схоже на необхідність перевірити сотні вимикачів, щоб дізнатися, який з них керує певною лампочкою», — каже Цююе Не, науковий співробітник лабораторії Гао й перший автор статті.
Як з’ясували дослідники, інша проміжна сполука, 2S-реміспорин A, що виробляється нещодавно ідентифікованим ферментом IscL, має атом сірки, який звисає з одного боку трикільцевої структури, подібно до зчіпного пристрою на задній частині вантажівки.
Від цвілі до медицини
Висока реактивна здатність циклопентахромону є джерелом його медичної універсальності: як вантажівка може перевозити різні типи причепів, зв'язок вуглецю та сірки у 2S-реміспорині A може об'єднуватися з широким спектром інших груп, утворюючи різноманітний набір молекул.
«Ця проміжна сполука дуже реактивна», — зазначає Не. «Зв'язок вуглецю й сірки може реагувати з різними донорами сірки, утворюючи безліч нових сполук».

Той факт, що 2S-реміспорин A настільки реактивний і може взаємодіяти з різними молекулами, навіть із самим собою, пояснює, чому цей попередник раніше ніколи повністю не ідентифікували.

«Ми ніколи не змогли б вигадати, як створити таку реактивну проміжну сполуку», — каже Не. «Нам довелося дослідити, як це робить природа, а потім самостійно використовувати ці ферментативні інструменти».
Дослідники сподіваються, що в майбутньому вони продовжать вивчення цього нещодавно відкритого шляху, використовуючи генетичну карту, яка допоможе їм розширити використання грибкових сполук у медицині.
«Природа має неймовірний набір інструментів», — каже Гао. «Ця стаття показує нам, як створюється один із таких інструментів».
До співавторів статті увійшли Чуньсяо Сунь, Шуай Лу й Марія Зотова з Penn Engineering, а також Цян Лі й Тун Чжу з Східно-китайського педагогічного університету.