Hola amigos

Fuente: @yusvelasquez
En el hogar, por ejemplo son varios los productos en donde se encuentra especificada en la etiqueta su concentración porcentual, ya que dependiendo del uso dependen sus características y la relación entre sus componentes. Sin embargo, puede que muchas veces no nos detengamos a revisarlas para conocer más en relación a sus componentes y a su concentración, lo cual resulta importante.
Revisemos algunos aspectos importantes desde el punto de vista químico que se deben dominar para la preparación de las soluciones. En primer lugar, recordemos que una solución se puede definir como una mezcla homogénea compuesta por dos o más sustancias, cuyos componentes principales son el soluto y el solvente. El soluto viene dado por la sustancia que se disuelve y el solvente la sustancia que disuelve.
A nivel de laboratorio, las disoluciones que más se emplean son las líquidas en donde el solvente más empleado es el agua. Ahora bien, cada solución tiene una cantidad de soluto y solvente establecido lo cual determina su concentración.

Fuente: @yusvelasquez
Existen varias forma de expresar la concentración de las soluciones, sin embargo nos enfocaremos en las unidades porcentuales que en forma general indican la cantidad de soluto en gramos o mL que se encuentran en 100 gramos o ml de solución. Entre ellas se encuentran el porcentaje masa-masa, porcentaje volumen-volumen y porcentaje masa-volumen.
Porcentaje masa/masa (%m/m)
Esta unidad expresa la cantidad de soluto en gramos que se encuentran en 100 gramos de solución. Por ejemplo, si se tiene una solución de cloruro de sodio NaCl 30% m/m, significa que 100 gramos de la solución está formada por 30 gramos de sal y 70 gramos corresponden al solvente.
El porcentaje m/m viene dado por la siguiente ecuación:
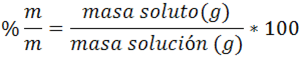
Si por ejemplo, en la cocina se mezclan 5 gramos de azúcar con 50 gramos de agua, la forma de determinar la concentración de esta solución es la siguiente:

Porcentaje volumen/volumen (%v/v)
Esta unidad expresa la cantidad de soluto en mililitros que se encuentran en 100 mililitros de solución. Por ejemplo, si se tiene un jugo con una concentración 40% v/v, significa que 100 mililitros de la solución está formada por 40 mililitros de zumo y 60 mililitros corresponden al solvente.
El porcentaje v/v viene dado por la siguiente ecuación:

Un ejemplo de la vida diaria donde se puede observar esta unidad de concentración es en el frasco de alcohol antiséptico que se puede adquirir en las farmacias. En este producto la etiqueta especifica 70 %v/v lo que expresa que contiene disueltos 70 ml del alcohol en 30ml de agua.

Fuente: @yusvelasquez
Por otra parte, si se desea preparar por ejemplo 500ml de esta solución al 70% los cálculos involucrados son los siguientes:

El cálculo muestra que para la preparación de la solución del alcohol se requieren 350ml de soluto.
El vinagre es otro ejemplo que se puede incluir, donde se especifica en la etiqueta un 5% de acidez.

Fuente: @yusvelasquez
Porcentaje masa/volumen (%m/v)
Esta unidad expresa la cantidad de soluto en gramos que se encuentran en 100 mililitros de solución. Por ejemplo, si se tiene una solución 20% m/v, significa que 100 mililitros de la solución está formada por 20 gramos de soluto y 80 mililitros corresponden al solvente.
El porcentaje m/v viene dado por la siguiente ecuación:
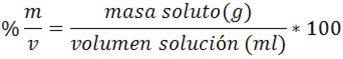
Si se desea preparar por ejemplo una bebida al 30% m/v con 20g del soluto concentrado, el cálculo del volumen de la solución vendrá dada por:
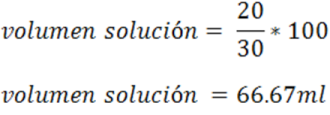
Esta unidad también es muy frecuente encontrarla en medicamentos como se muestra

Fuente: @yusvelasquez
Como vemos, la información mostrada sirve como herramienta para la preparación de las soluciones a diferentes concentraciones para diferentes fines, así como también para interpretar el contenido de un producto que se desea usar.
Bueno amigos, espero la información mostrada les sea de gran utilidad, hasta una próxima oportunidad, gracias por leer!
Referencias
- Soluciones químicas
- Whitten K. y Gailey, K. (1985). Química General. México: Nueva Editorial Interamericana
Un post muy informativo gracias por compartir tus conocimientos, saludos amiga!
Hola @marile21, gracias por pasar a leer!
Thanks for your contribution to the STEMsocial community. Feel free to join us on discord to get to know the rest of us!
Please consider delegating to the @stemsocial account (85% of the curation rewards are returned).
You may also include @stemsocial as a beneficiary of the rewards of this post to get a stronger support.
¡Gracias por el apoyo!