Saludos amigos amantes de la ciencia...
En esta oportunidad presentare la continuación de mi primera entrega, donde compartía una breve introducción del análisis térmico. Sabemos que son un conjunto de técnicas mediante las cuales podemos analizar la variación de las propiedades físicas y químicas en función de la temperatura.

Estas técnicas tienen una amplia aplicación en lo que respecta a minerales, metales, aleaciones, plásticos, semiconductores, sustancias, medicinas. Todo esto sirve como control de calidad de todos los productos derivados de los ya mencionados.
El objetivo de este artículo es dar a conocer un poco sobre uno de los métodos más usados en este tipo de análisis térmico.
Método de análisis termogravimétrico

Configuración experimental: instrumento de termogravimetría con horno EGA. Licencia CC BY 4.0 de wikipedia
En este método incluye todas aquellas formas de análisis en la que se produce una medida de la variación de la masa cuando está sometida a cierta temperatura, ya sea constante que registra la calefacción en función del tiempo, como por ejemplo puede ser un proceso de secado a una temperatura de 100ºC. Entonces el registro de la pérdida de masa que presenta el material se realizara en función del tiempo.
También podemos realizar un registro de la variación de la masa del material que se desea analizar a una temperatura variable, en este método el registro final lo podemos realizar en función del tiempo o también en función de su temperatura, para ambos casos el resultado final de la medida trae como resultado un termograma que se identifica con la curva de descomposición térmica.
Las mediciones de cambio de masa con respecto a su temperatura se realizan en una termobalanza la cual está conformada por los siguientes elementos:
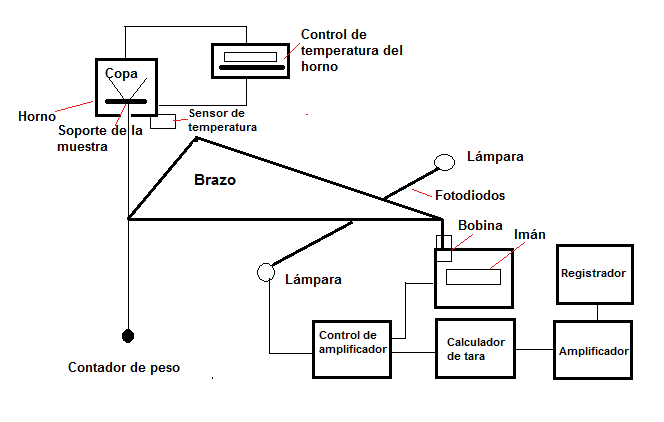
La parte esencial para este equipo de termogravimetría es la balanza y el horno. En el caso de la balanza, esta debe ser lo suficientemente precisa para medir muestras con un peso de 1-100mg con una estimación de 0,0004mg. En esta también se asegura que la muestra a medir permanezca en la misma zona en la que se encuentra el horno, a pesar de la variación de la temperatura. El movimiento del brazo en la micro balanza de un punto muerto se usa en un aparato electro-óptico con un regulador de entrada de luz que está unido al extremo del brazo.
Otro punto muy importante a destacar es que el movimiento del brazo de la balanza altera la intensidad de la luz que entra a la fotocelda, esta misma genera una señal que se amplifica y restaura la posición del brazo en un punto muerto, al mismo tiempo que mide el cambio de masa de la muestra. La señal eléctrica de salida se transforma en una curva derivada termogravimétrica.
El horno juega un papel fundamental en este sistema de medición, en este se sitúa un platillo que es donde estará arrojada la muestra, el horno debe tener una capacidad de medir desde temperatura ambiente hasta temperatura elevadas de unos 1500ºC, y también debe ser capaz de controlar de forma muy precisa el calentamiento de la muestra.
Además, en la gran mayoría de las termobalanzas, los hornos están constituidos de un intercambiador de gases que nos permite realizar la calefacción en diferentes tipos de atmósferas, es por ello que este sistema contiene a su vez un sistema de gases, dichos gases pueden ser inertes como el nitrógeno y el argón. También oxidantes como el oxígeno y el aire y de igual forma reductores como por ejemplo el hidrógeno. El intercambio de los gases durante el proceso de calefacción nos da como resultado un tipo de descomposición o reacción química diferentes.
Las termobalanzas también están compuestas de un microprocesador que nos permite controlar de forma fácil el equipo de medición y la adquisición de todos los datos que se van produciendo.
Y finalmente un software que también es muy sencillo de usar que nos permite el manejo del equipo y el tratamiento de los datos obtenidos.
Aplicaciones del análisis termogravimétricos
Presenta una gran variedad de aplicaciones. Un ejemplo claro es el carbón bituminoso a través de la utilización de gases durante el proceso de calefacción.
El carbón bituminoso es un carbón relativamente duro que contiene betún, entre el lignito y la antracita en la serie ligno-hullera. Suele ser de color negro, a veces marrón oscuro, presentando a menudo unas bandas bien definidas de material brillante y mate. Las vetas de carbón bituminoso se identifican estratográficamente por la distintiva secuencia de bandas brillantes y oscuras.
En la siguiente gráfica podemos observar una curva TG, que viene siendo la curva con un trazo continuo, por lo contrario, la curva con el trazo discontinuo es correspondiente con el programa de temperatura. Inicialmente al comienzo del tratamiento al aumentar la temperatura a 110ºC, donde luego se produce la perdida de agua y a partir de ahí aumenta la temperatura hasta los 950ºC donde se produce la eliminación de la materia volátil en la muestra, todo esto debido a que se produce en una atmósfera de nitrógeno, es decir un gas inerte.
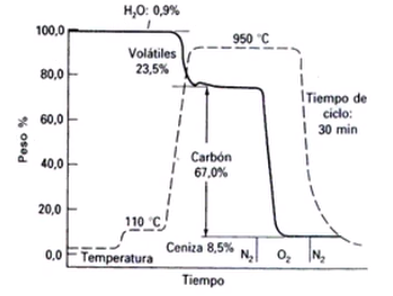
Una vez que alcanzamos una zona de un peso constante en la curva TG se procede al cambio de la atmósfera, es decir se introduce una atmósfera oxidante que trae consigo un salto que corresponde a la pérdida del carbón del material que estamos analizando.
Este método también es muy utilizado en el estudio de polímeros o materiales poliméricos. Para el estudio de este tipo de materiales se siguen las mismas condiciones de calefacción con que cada material polimérico sigue una curva diferente de descomposición, por lo cual no solamente nos sirve para análisis si no en algunas ocasiones como método de identificación.
De igual forma podemos utilizar esta técnica para determinar el contenido de distintas sustancias dentro de una muestra, como por ejemplo en él estudio el contenido de un carbono y un polietileno.
Se utilizan para el estudio de materiales inorgánicos, como por ejemplo en la descomposición del CaCoO+H2O en una atmósfera inerte.
Para este caso es común que los compuestos inorgánicos den lugar a una curva de descomposición térmica en la cual la reacciones se dan de forma sucesivas o de forma escalonada como se muestra en la siguiente gráfica.
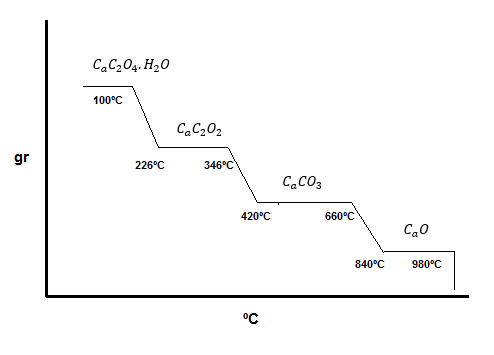
El primero corresponde a un salto corresponde a la reacción de deshidratación de Ca Co O+ H2O por perdida de una molécula de agua, es decir Ca C2 O3 + H2O.
El segundo salto en la gráfica es correspondiente a la descomposición del Ca C2 O+ = por perdida de una molécula de oxígeno, Ca CO3 + CO.
Y finalmente el tercer salto corresponde con la descomposición del Ca CO3 = CaO + CO2.
Entonces esto se traduce a que cada una de estas reacciones dan lugar a compuestos con una estequiometria perfecta, mediante el cual es posible relacionar el contenido de estos compuestos con la cantidad de material que se ha podido eliminar de la muestra analizada.
Otro ejemplo podría ser el análisis de mezclas de alcalinos, mediante la cual podemos observar en la siguiente gráfica una mezcla de oxalatos de calcio, bronzio y bario, donde cada uno de estos compuestos producen una descomposición a diferentes temperaturas.
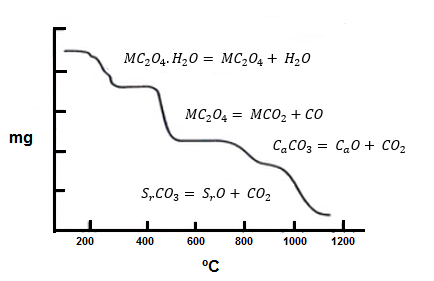
En el primer salto correspondiente a la perdida de una molécula de agua por formula, los oxalatos experimentan una reacción a un intervalo de temperatura bastante aproximado, sin embargo, se puede observar que cada uno de le da lugar a un salto totalmente diferente, por lo cual no pueden desprenderse.
El segundo salto que corresponde a la reacción de descomposición de carbonatos, los tres oxalatos, dan lugar a una reacción a la misma temperatura, en el cual se distingue solo un salto.
Y finalmente el tercer salto que corresponde a la descomposición de los óxidos, dan lugar a diferentes temperaturas para cada uno de los metales y se pueden visualizar claramente el salto de cada uno de los compuestos.
Importante destacar un caso especial en este tipo de análisis, y es que cuando las curvas termogravimétricas no se puedan observar lo saltos de forma clara se usa el "termograma diferencial", que viene siendo la curva derivada de la curva termogravimétrica. Ya que en ella se podrían distinguir de forma fácil todos los puntos de descomposición.
En resumen podemos decir que es un método muy útil para identificar descomposiciones, transiciones de diversos compuestos químicos. En este post me centre en explicar cómo está conformado el equipo, cuáles son sus diferentes componentes y cuál es la función de cada uno de ellos dentro de la termobalanza. De igual forma se explica en detalle algunos ejemplos de diferentes sustancias químicas para el análisis de los resultados de su correspondiente termograma.
Fuente de imágenes de portada
Para más información
No olvides votar por @stem.witness como testigo
Ahora puedes escribir tus publicaciones a través de la app oficial https://www.steemstem.io y obtendrás un voto extra del 5%
@STEM-Espanol tiene su nueva página de twitter. Así que no olvides y visitarla y seguirnos!

https://twitter.com/EspanolStem

Saludos estimado @carloserp-2000. Es interesante el estudio que nos presentas. No había oído a cerca de esto. La gravimetría es empleada en varias áreas para determinar ciertos comportamientos, especialmente, de materiales inorgánicos. Y se basa principalmente en la variación de la componente vertical de la aceleración de la gravedad terrestre. Sin embargo, los estudios en función de altas temperaturas y en función de esta variable estaban fuera de mis conocimientos. Que bueno es poder tener personas que nos explican estas cosas.
Entiendo la parte donde la masa es vital para el desarrollo de esta técnica experimental. Sin embargo la Fuerza gravitacional creo que es la protagonista en esta técnica en conjunto con la temperatura. Y claro ambas estan relacionadas sin embargo, la fuerza gravitacional cambia de acuerdo con la posición geográfica, por el contrario, la masa no. Tu que piensas de esto?
Saludos.
Gracias por explicar las partes del equipo de análisis de TGA @carloserp-2000. En el termograma del carbón bituminoso, después de perder el 23.5% del peso se observa un incremento nuevamente en el peso. ¿Cómo se podría explicar ese fenómeno? Saludos
Hola @ritch si puedes observar detalladamente el gráfico, eso que acotas no sucede!. A medida que se va aumentando la temperatura el carbón va perdiendo su masa. En este caso cuando tenemos una atmósfera de gas inerte >(nitrógeno) el carbón alcanza un peso constante. Posteriormente al cambiar de atmósfera a un gas oxidante corresponde a una perdida del mas del 60% de carbón, luego volvemos a cambiar la atmósfera y el peso se vuelve a mantener constante. El detalle esta en observar bien la gráfica jeje
Gracias @carloserp-2000. Creo que el pequeño aumento en el peso se podría deber al cambio del gas de arrastre, cómo lo mencionas. Jeje
Posted using Partiko Android
This post has been voted on by the SteemSTEM curation team and voting trail. It is elligible for support from @utopian-io.
If you appreciate the work we are doing, then consider supporting our witness stem.witness. Additional witness support to the utopian-io witness would be appreciated as well.
For additional information please join us on the SteemSTEM discord and to get to know the rest of the community!
Thanks for having added @steemstem as a beneficiary to your post. This granted you a stronger support from SteemSTEM.
Thanks for having used the steemstem.io app. You got a stronger support!
Hi @carloserp-2000!
Your post was upvoted by Utopian.io in cooperation with @steemstem - supporting knowledge, innovation and technological advancement on the Steem Blockchain.
Contribute to Open Source with utopian.io
Learn how to contribute on our website and join the new open source economy.
Want to chat? Join the Utopian Community on Discord https://discord.gg/h52nFrV