Hidroformilación de olefinas
La hidroformilación de olefinas, también conocida como proceso OXO, es una de las reacciones catalíticas más importantes a nivel industrial, ya que permite obtener una amplia variedad de moléculas orgánicas de alto valor comercial (aldehídos y alcoholes) y es también una de las aplicaciones de gran escala de la catálisis homogénea en la industria. Esta reacción consiste en la adición de una mezcla de hidrógeno y monóxido de carbono (gas de síntesis), en forma de un átomo de hidrógeno y de un grupo formilo, al doble o triple enlace carbono-carbono de una olefina, dieno, acetileno o de otros compuestos insaturados.(1,2)
En el proceso experimental de la reacción de hidroformilación de olefina del presente proyecto investigativo, no se llevó a cabo mediante el uso de gas de síntesis como tradicionalmente, se emplea para este tipo de reacción. Sino, que por el contrario se decide; emplear otra forma de lograr la hidroformilación de una olefina a sus correspondientes aldehídos. Mediante el uso de formaldehído como fuente de un átomo de hidrógeno y de grupo formilo (HCO). El uso de paraformaldehído en lugar de gas de síntesis en la reacciones de hidroformilación presenta tres ventajas fundamentales con respecto al proceso clásico: 1) se evita el uso del gas letal monóxido de carbono; 2) en el proceso se pueden utilizar sistemas más sencillos (balones de vidrio o ampollas) ya que no se requieren altas presiones de un gas, y 3) una forma más simple de las cinéticas y los mecanismos.
La importancia de este tipo reacción radica en que es uno de los procesos catalíticos homogéneos de mayor interés en la industria es la hidroformilación de olefinas o proceso OXO, en el cual se generan aldehídos con un átomo de carbono más que el alqueno de partida. En el caso de una olefina terminal con una cadena carbonada de tres o más átomos de carbono, existen dos posibles productos de reacción: el aldehído lineal o normal (n) y el ramificado o isoaldehído (i). La reacción produce además alquenos internos (excepto en el caso del propeno) y alcanos, a causa de la isomerización e hidrogenación de la olefina, respectivamente, y alcoholes por la hidrogenación de los aldehídos producidos.(1)
Como se ha establecido hasta ahora, la reacción de hidroformilación empleando una mezcla de CO/H2 se ha erigido como el proceso industrial más importante para la obtención de aldehídos a partir de olefinas. No obstante, existe un proceso alternativo a la hidroformilación de alquenos con gas de síntesis, que se basa en el uso de paraformaldehído en combinación con complejos de metales de transición. En esta reacción (un caso particular de hidroacilación de olefinas, con R´=H), el paraformaldehído actúa como fuente de hidrógeno y del grupo formilo.
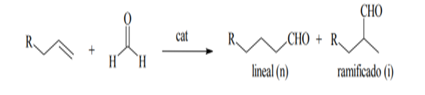
Figura 1. Proceso de síntesis empleando formaldehido. Fuente: elaboración propia
PROCEDIMIENTO EXPERIMENTAL
Síntesis del complejo de CoCl(PPh3)3
El complejo CoCl(PPh3)3 se sintetizo empleando la metodología reportada por Cotton para el análogo organosoluble. Se desoxigenaron 10mL de Etanol, se disolvieron 661mg de (PPh3) y 300mg de CoCl2.6H2O en el etanol. La solución se introdujo en un balón de tres bocas provisto de sistema de agitación, calentamiento y condensación. Se agito la mezcla en reflujo por cuatro horas, al final de las cuales se enfrió la solución, y finalmente se evaporo el etanol en vacío para obtener los cristales de color azul.
Reacción de hidroformilación de eugenol catalizada por CoCl(PPh3)3.
La reacción catalítica de hidroformilación de olefina con formaldehído se realizó en un vaso de reactor de vidrio Fischer Porter de 50 mL, el cual se introdujo en un autoclave de acero Parr Instruments de 125 mL, modelo 4561, el mismo se encuentra provisto de un puerto para la extracción de muestras y acoplado a una consola en la que se puede realizar el control digital de la presión, la temperatura y la velocidad de agitación de la mezcla de reacción. Esto se llevó a cabo colocando en un vaso de vidrio dentro del reactor de acero: 0,052g pre-catalizador, 1,3171g de sustrato, 0,5239g de para formaldehido y 40ml de dioxano como solvente. Posteriormente, el reactor se calentó a la temperatura de reacción deseada. Para finalizar Se tomaron muestras de la mezcla de reacción y se analizaron mediante cromatografía en capa fina (TLC). Para analizar la composición de las mezclas catalíticas. Tanto de la mezcla inicial, como de la mezcla obtenida al finalizar la reacción de hidroformilación. Al final de la reacción, el reactor fue enfriado en baño de hielo y ventilado lentamente antes de abrirlo.
Caracterización del producto obtenido de la reacción de hidroformilación, empleando el método de (TLC).
Las muestras se aplicaron sobre las placas a 1 cm de distancia del borde de la misma mediante el uso de un capilar muy fino, realizando varias aplicaciones, secando la muestra sembrada después de cada aplicación. Una vez secada la muestra en la placa, ésta se llevó a la cámara de desarrollo y posteriormente a la cámara de revelado. Para esto se colocó en el interior de la cámara suficiente solvente (Cloroformo) como para cubrir el fondo hasta una altura aproximada entre 0.3 a 0.5 cm. Y finalmente se tapó; Cuando el frente del solvente alcanzo una posición aproximada de 0.5 cm del borde superior del adsorbente, se retiró la placa.
Después del desarrollo, se marcó el frente del solvente con un lápiz y se dejó evaporar el solvente. Para el revelado con yodo, se colocaron unos cristales en un beaker y posteriormente se taparon con un vidrio de reloj, se esperó hasta que se hiciera visible el vapor púrpura. Cuando se evaporo el solvente de la placa TLC, se colocó con cuidado en la cámara de yodo y se tapó, en unos segundos. Se observó la aparición de las manchas, continuamente se sacó la placa de la cámara de revelado y se marcó en el centro de la mancha, esto fue preciso debido a que las mancha desaparecían a medida que se evaporo el yodo. Para revelar grupos carbonilo se roció con 2,4-dinitro-fenilhidrazina.
Cálculos Teóricos
Los cálculos teóricos realizados al complejo CoCl(PPh3)3 se llevaron a cabo utilizando la Teoría del Funcional de la Densidad (DFT) mediante la aplicación del programa GaussView, de la cual se tomó el resultado del espectro infrarrojo (IR) para la determinación de la geometría del complejo, el cual también fue comparado con el espectro infrarrojo experimental, obtenidos mediante técnicas tradicionales de espectroscopia infrarroja.
RESULTADOS Y DISCUSIÓN
En este trabajo se evaluó la actividad catalítica del sistema formado por la reacción de cloruro de cobalto hidratado (CoCl2.6H2O) con tres ligandos de PPh3. El estudio se inició evaluando si se lograba obtener producto, mediante la reacción de hidroformilación de olefinas; y si esta era posible con un método no convencional utilizando paraformaldehido en lugar de gas de síntesis, lo cual daría el producto final a sus correspondientes aldehídos. El Eugenol en la reacción fue tratado con una temperatura de 150ºC, sin la distribución de gas de síntesis. Con 1000rpm; 4 h de reacción; 32, 72 mg del catalizador; Dioxano 40mL.
Se presume como producto de reacción, la obtención de un aldehído lineal, debido a que el proceso de reacción de hidroformilación se llevó a cabo mediante el empleo de un complejo del cobalto modificado, CoCl(PPh3)3, aunque tradicionalmente, los catalizadores preferidos en plantas industriales han estado basados en carbonilos de cobalto. En su forma no modificada, se introduce en el reactor como octacarbonilodicobalto, Co2(CO)8, sales de cobalto (II) o cobalto metálico, que bajo las condiciones de reacción, típicamente 100-120 ºC y 100-300 atm de presión de gas de síntesis (H2 + CO), se transforman en la especie activa HCo(CO)n, n=3,4; este sistema es altamente activo, produciendo aldehídos con relaciones lineales: ramificado (relación n/i) en el rango 3-4.
La proporción de productos lineales ha sido mejorada notablemente, modificando el catalizador mediante la substitución de un grupo carbonilo por ligandos más adecuados como Trifenilfosfina para el desarrollo de un sistema catalítico homogéneo eficiente y selectivo para la hidroformilación de olefinas. Además generalmente se desea una alta selectividad para la obtención de aldehídos lineales; ante la presencia de aldehídos ramificados y otros productos secundarios. Por otra parte también se puede inferir la obtención de un aldehído debido a que se empleó paraformaldehído como fuente de un átomo de hidrógeno y de grupo formilo (HCO). Lo cual imposibilita la formación de alcoholes, en este mismo sentido también se puede asegurar que el producto de reacción obtenido presenta al menos la presencia de un grupo carbonilo, debido a que en el proceso de revelado de la placa de cromatografía al rociar con una solución de 2,4-dinitro-fenilhidrazina este; dejo observar una mancha como posible producto dehidroformilación, seguidamente se procedió a la realización comparativa de la reacción de la solución indicadora con bencylacetona de la cual se destacó la formación de un precipitado de un color similar, al que se encontraba presente en la placa de TLC, cabe destacar que se descartó que fuese presencia de solvente de la reacción debido a que se realizó la misma prueba de la solución con el paraformaldehido con dioxano notándose que esta permanecía inalterable, con el mismo color y estado líquido característico de la solución de 2,4-dinitro-fenilhidrazina.
Mediante la determinación de los cálculos computacionales se pudo conocer el espectro infrarrojo teórico. Figura 1, donde las señales en 3300cm-1 corresponde a la tensión del anillo aromático, entre 2000-2500 cm-1 muestra la flexión de H de las fosfinas, en 1500cm-1 corresponde a los sobretonos de los enlaces H de las fosfinas, en 1200cm-1 y 1000cm-1 son las flexiones de H (monosustituido) y en 500cm-1 corresponde a los sobretonos del anillo aromático.

Figura 2. Espectros (IR) teórico del complejo de CoCl(PPh3)3. Fuente: elaboración propia
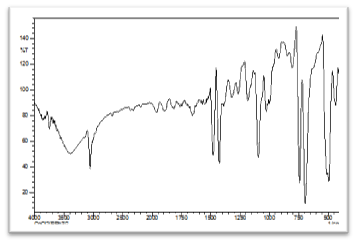
Figura 3. Espectros (IR) experimental del complejo de CoCl(PPh3)3. Fuente: elaboración propia
CONCLUSIONES
El sistema CoCl(PPh3)3 resultó ser activo para la reacción de hidroformilación de Eugenol, debido a que mediante el análisis de (TLC)que el producto obtuvo actividad catalítica, por cuestiones del tiempo de realización del presente proyecto. No se determinó con mayor exactitud, que es el producto de resección formado. Aunque por teoría se sabe, que se espera la obtención de un aldehído lineal; debido a que se empleó un complejo modificado de cobalto la cual debiera de mostrar una alta selectividad en la obtención de aldehídos lineales antes de ramificados. En este mismo sentido, también, se pude inferir la presencia de grupos carbonilos en el producto de reacción obtenido de hidroformilación, debido a que en el proceso de revelado de las placas de (TLC) se empleó 2,4-dinitro-fenilhidrazina el cual, se emplea únicamente en el revelado de grupos carbonilos, resultando esté reaccionante en el producto obtenido.
Para obtener una mayor exactitud en la caracterización del producto obtenido, se recomienda continuar con los análisis pertinentes. Que permitan afianzar de forma más técnica, precisa y confiable la presencia de un aldehído, como por ejemplo mediante la aplicación el método HPLC, cromatografía de gases. U otro análisis químico, que se considere pertinente en dicha determinación. En este mismo sentido también se recomienda llevar a cabo el análisis para determinar el porcentaje de conversión obtenido. En el sistema, de Co/PPh3 para la hidroformilación de eugenol.
REFERENCIAS BIBLIOGRAFICAS
- Collman, J. P.; Hegedus, L. S.; Norton, J. R.; Finke, R. G., 1988, Principles and applications of organotransition metal chemistry, California, EUA, University Science Book, pp. 619- 659.
- Bhaduri, S.; Mukesh, D., 2000, Homogeneous catalysis. Mechanisms and industrial applications, New York, USA, Jhon Wiley and Sons Publications, pp. 85-98
- Ritleng, V.; Siriln, C.; Pfeffer, M., 2002, “Ru-, Rh-, and Pd-Catalyzed C-C Bond Formation Involving C-H Activation and Addition on Unsaturated Substrates: Reactions and Mechanistic Aspects”, Chem. Rev., 102, 1731-1769
- Ahn, H. S.; Han, S. H.; Uhm, S. J. ; Seok, W. K.; Lee, H. N.; Korneeva, G. A., 1999, “Hydroformylation of olefins with formaldehyde in the presence of RhHCO(PPh3)3”, J. Mol. Catal. A, 144, 295-306.
- Ahn, H. S.; Han, S. H.; Uhm, S. J. ; Seok, W. K.; Lee, H. N.; Korneeva, G. A., 1999, “Hydroformylation of olefins with formaldehyde in the presence of RhHCO(PPh3)3”, J. Mol. Catal. A, 144, 295-306.
- COTTON F.A., FAUT O.D., GOODGAME D.M.L., HOLM R.H. J AmerChemSoc83:1780-1785. 196.
Hola estimada @mayterevilla. Estas experiencias practicas te llevaran a tu completa formación profesional. Saludos
¡Felicitaciones tu publicación ha sido seleccionada para recibir el Upvote y Resteem del Proyecto de Curación @Codebyte!
Para saber mas sobre este proyecto puedes seguirlo y estar atento a sus publicaciones. No olvides votar este comentario para recibir mejores ganancias en el futuro y revisar tu post en el reporte diario LINK.
Congratulations @mayterevilla! You have completed some achievement on Steemit and have been rewarded with new badge(s) :
Click on any badge to view your own Board of Honor on SteemitBoard.
To support your work, I also upvoted your post!
For more information about SteemitBoard, click here
If you no longer want to receive notifications, reply to this comment with the word
STOPHola May, creo que hice una práctica parecida mientras estudiaba pregrado, aunque creo que no la recuerdo porque siempre le he huido a la catálisis homogénea jajaja. Yo trabajé en heterogénea en mi tesis de grado, específicamente una alquilación Friedel-Crafts sobre unos sólidos mesoporosos. Me gustó tu artículo, bien explicadito, te deseo éxitos futura colega.
Muchísimas gracias @oscardice voy a pasarme por tu perfil en cualquier momento, saludos!