
출처: Pixabay
저작권: Creative Commons 0
안녕하세요, @doctorbme 입니다.
오늘은 연구 이야기에 앞서서, 사람 대상 연구를 하기 위해 필요한 윤리적 이슈들을 이야기 하기 위해, Informed Consent (사전 동의, 알려 준 후의 동의) 에 대해서 살펴보고자 합니다.
인공기관지와 어느 의사의 스캔들과 관련한 글을 읽고 한번쯤 적어보면 좋겠다 싶어서 작성하는 글입니다.이 글은 @junn 선생님의
기본적으로 사람을 대상으로 하는 연구를 시행하기 위해서는, 기본적으로 연구 시작 전에 연구윤리심의위원회(이하 IRB)의 승인을 받아야 합니다. 이러한 과정에서 사전 동의 (Informed consent)를 받기 위한 설문지를 제출하기도 하며, 실제로 IRB 승인을 받은 이후에 각 피험자들(혹은 환자들/연구에 참여한 일반인들)에게 사전 동의(Informed Consent)를 꼭 받아야 합니다.
여기서 IRB란, 간략히 설명드리자면,
연구에 참여하는 연구대상자 (피험자)의 권리와 안전, 그리고 복지를 위하여 연구의 윤리적, 과학적 측면을 심의하여, 연구의 계획을 승인할 수 있는 독립된 합의제 의결기구
라고 볼 수 있겠습니다.

저작권: CC BY-SA 3.0
출처: https://en.wikipedia.org/w/index.php?title=File:PARAMOUNT_Eli_Lilly_Informed_Consent_Document.djvu&page=3
사전 동의의 한 페이지를 나타냅니다. 굵은 글씨로 어떤 위험과 부작용이 가능한지에 대한 항목 그리고 이에 대한 설명이 이어집니다.
이러한 사전 동의 (Informed consent) 는 아래와 같은 의미를 가집니다.
- 실제 행위가 어떻게 이루어지는지에 대한 이해를 바탕으로, 행위에 대한 승인
- 사람을 대상으로하는 연구에 요구되는 법적, 규율적, 윤리적 필수 조건
- 이성적인 의사결정의 한 과정
- 윤리적인 임상 연구 시행을 위한 요건
요약하자면, 결국 사람을 대상으로 하는 연구에 있어서 피험자가 어떠한 행위를 받을지 이해하고 동의를 하는 과정을 뜻합니다.
그렇다면 이를 위해서는 어떠한 요소를 갖추어야 할까요?
- 정보의 공개 (disclosure of information)
- 이해 (understanding)
- 자발성 (voluntariness)
- 동의의 공식적인 허가 (consent authorization)
최소한 위의 네 가지 요건이 충족되어야 합니다.
우선 정보의 공개를 살펴보겠습니다.
정보의 공개를 하는 입장( 연구자)의 입장에서는 아래의 사항을 고려해야 합니다.
- 얼마나 많이 그리고 어떤 정보를 공개해야할 것인가?
- 이러한 정보를 어떻게 나타내야할 것인가?
- 정보를 공개할 때의 환경은 어떠한가?
보통 서면으로 작성된 사전동의서 형태를 취하고, 이 안에 정보를 넣는 경우가 많습니다.
이를 위해서는 연구가 어떠한 목적을 가지고 있고 어떤 과정을 통해 진행되며, 이떄 관여하는 위험과 가능한 부작용, 그리고 얻을 수 있는 이익 등을 기술합니다. 하지만 종종 아래와 같은 도전에 부딪히기도 합니다.
- 대부분 연구 사전동의는 서면 형태로 작성되어 있어서 굉장히 길고 복잡하며 소통하기 어려움
- 사전동의서가 연구자 혹은 연구 기관을 보호하는 목적으로 사용되는 경우도 있음
이해(understading)은 사실 연구를 위한 사전동의를 받는데에 있어서, 피험자들이 겪는 가장 큰 어려움일 것입니다. 얼마나 적절한 정보를 전달할 수 있으며, 또한 이러한 정보가 실제로 잘 받아들여졌는지 파악하기 어렵기 때문입니다.
이를 해결하기 위해서는 아래와 같은 방안들이 고려됩니다.
- 비디오, 컴퓨터를 통한 도구 활용
- 포맷이나 길이, 가독성을 높인 사전동의서 구성
- 연구자 혹은 중립적인 교육자를 통한 추가적인 교육 및 토론
- 퀴즈 혹은 리뷰를 통한 테스트와 피드백 (하지만 테스트를 받는 것을 좋아하는 피험자는 없으시겠죠...)
하지만 사전 동의에서 제일 중요한 것은 바로 자발성 입니다. 피험자는 언제나 연구 참여를 거부할 권리가 있고 누구든 이에 대해 강제하거나 부당한 압력을 행사할 수 없습니다. 그리고 없어야 합니다.
이러한 자발성에 영향을 끼칠 수 있는 요인으로는,
의존적인 관계, 권력/수직 관계 (황우석 사태를 떠올려보면 됩니다. 연구원들이 난자를 기증해야 했습니다.) , 연구자에 대한 신뢰, 질병 (임상시험을 해서 신약을 받아야 하는 경우 등), 금전적 요인 (임상 시험에 참여해서 여러 이득을 볼 수 있는 경우) 등
이 있습니다.
아직까지 사전 동의의 경우
- 사전 동의 양식이 길고 복잡하고 어려움
- 피험자의 경우, 연구에 대한 이해도가 다르거나 부족할 수 있음
- 많은 참가자들이 이미 시작한 사전 동의를 철회하거나 중단하는 것에 심리적 부담을 느낄 수 있음
과 같은 경우가 발생할 가능성이 있기 때문에, 이에 대한 여러 노력들이 필요하기도 합니다.
연구 참여 시에는 항상 사전동의서를 꼼꼼히 읽으시고 궁금한 사항을 가지고 계시면 질문과 소통을 통해 충분한 이해와 자발적인 참여가 이루어지기를 희망합니다. 또한 참여자의 경우 언제라도 중단 및 거부할 수 있는 권리가 있음을 알아두시면 좋을 것 같습니다.
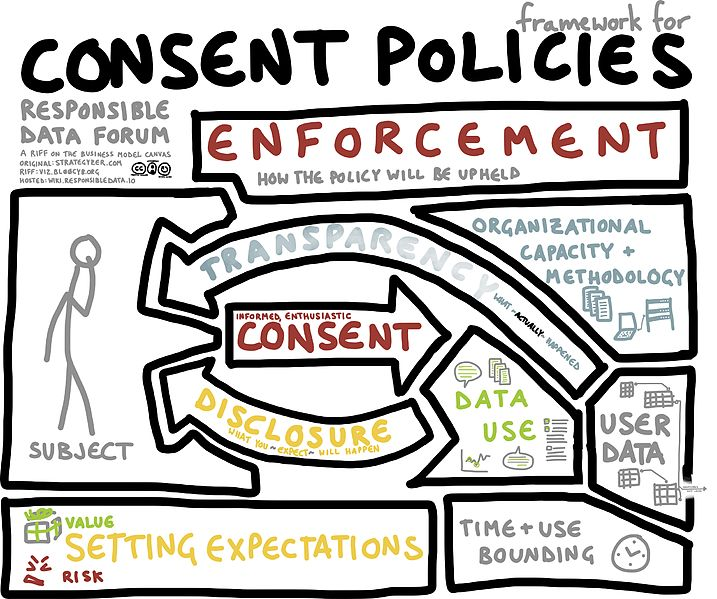
출처: Wiki Framework for Consent
저작권 : CC - BY -SA 4.0
최근 데이터를 다루는 연구에 있어서는,
(사전 동의를 거친) 나의 데이터가 어떻게 쓰이고 있는지 투명성을 통해 접근 가능한 것도 중요한 이슈입니다.
사전 동의를 거치고 데이터를 생산하는 객체로서 그치는 것이 아니라, 실제로 이렇게 생성된 데이터가 연구 과정에서 어떻게 기여하고 있고, 이를 통해 어떠한 이득과 위험을 가질 수 있는지를 전달 받고 행위할 수 있는 주체로서의 피험자의 역할도 강조되고 있습니다.
참고문헌 (Reference)
[1] NIH, Ethical and Regulatory Aspects of Clinical Research
[3] 김옥주, 실험적 연구에서 생명윤리와 개인정보 보호, 한국역학회지, Vol 29, No 1. 2007
[2] 서울대병원 임상연구윤리센터, http://hrpp.snuh.org/irb/introirb/_/singlecont/view.do

오늘도 잘 읽고갑니다 선생님~
선생님께서 말씀하신 모든 부분들을 피험자들이 알면 좋겠지만 위의 언급한 부분만큼은 정말 모든 이들이 알아둬야할 사항이 아닌가 싶네요. 다음글 기대하겠습니다. 좋은 하루되세요!
감사합니다. 사실 자발성 만큼이나 복잡하고 건드리기 어려운 이슈도 드물겁니다. 자발적인 것과 자발적이지 않은 것 사이의 경계가 모호할 때가 있습니다.
예를 들어
이러한 케이스들을 생각해볼때, 사실 자발성은 그 이면에 피험자들을 둘러싼 배경을 살펴보아야하기에, 항상 조심해야한다고 생각합니다. 이러한 측면에서, 참여자들이 가지는 권리는 최소한의 장치라 생각됩니다. :)
좋은 글 감사드립니다~ 쓰기 쉽지 않은 내용을 너무 잘 정리해주신 것 같아 조심스레 제 글에다 이 포스팅을 링크를 포함시켜두겠습니다ㅎ
넵. 선생님 덕분에 저도 한번쯤 이야기하고 싶었던 소재에 대해서 정리하면서 글을 적어볼 수 있었습니다. 감사합니다.